君实生物(01877):中和抗体海外临床数据良好,上市可期
本文来自微信公众号“向阳论医谈药”,作者: 西南证券医药团队。
投资要点
事件:10月7日,礼来公司(LLY.US)宣布其SARS-CoV-2中和抗体项目的轻中度卫生事件的患者联合治疗的中期数据。
中和抗体联用方案(LY-CoV555和LY-CoV016)显著降低病毒载量和就诊率。BLAZE-1临床试验的中期数据表明,联合使用两种SARS-CoV-2中和抗体可以降低体内病毒载量,减轻相关症状,同时降低住院和急诊风险。探索性分析显示,与安慰剂组(20.8%)相比,联合治疗组在第7天较高病毒载量的患者比例显著较低(3.0%)。此外,与安慰剂组(5.8%)相比,联合治疗的患者住院或急诊的就诊率较低(0.9%),相对风险降低84.5%(p=0.049)。
礼来公司预计第四季度开始生产联合用药中和抗体。为了尽快提供患者可及药物,即使尚未有数据显示这两种抗体疗法可能成为卫生事件有效疗法,礼来仍在大规模投资生产这两种抗体。针对单一疗法,公司预计在2020年第四季度将提供超过100万剂700mg的LY-CoV555用于单一疗法,其中10万剂将可能于10月上市。至于联合疗法,预计2020年第4季度将可能提供5万剂该抗体。从2021年第一季度开始,公司将可能大幅增加联合疗法药品的供应。
君实生物(01877)对LY-CoV016的海外权益享有里程碑付款及销售分成。礼来进行试验的两个中和抗体中。LY-CoV555是礼来与AbCellera公司合作开发的用于预防和治疗患者的中和抗体。LY-CoV016(又称JS016)是礼来与君实生物、中国科学院微生物研究所合作的针对患者的中和抗体,其海外权益授权给礼来公司,公司获得1000万美元首付款,不超过2.45亿美元的里程碑付款,外加该产品销售净额两位数百分比的销售分成。
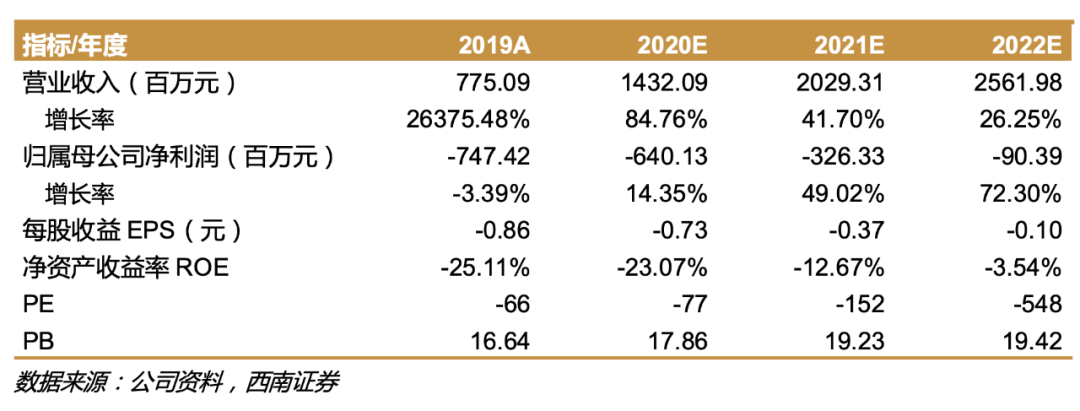
盈利预测与评级。预计公司2020-2022年EPS分别为人民币-0.73/-0.37/-0.10元。公司与中国科学院微生物研究所及礼来公司合作的中和抗体在临床试验中显示出良好的效果,体现出公司研发的高效率,如该产品能成功上市,将有望增厚公司业绩。维持“买入”评级。
风险提示:1)中和抗体及在研管线研发进展不及预期;2)特瑞普利单抗产品降价幅度超预期;3)特瑞普利单抗以及未来上市产品不能进入医保的风险。
(编辑:张金亮)



 扫码下载智通APP
扫码下载智通APP