新股消息 | 潜在的领先双抗平台,康方生物(09926)研发能力获国际领先制药公司认可
本文来自微信公众号“国泰君安证券香港”,文中观点不代表智通财经观点。
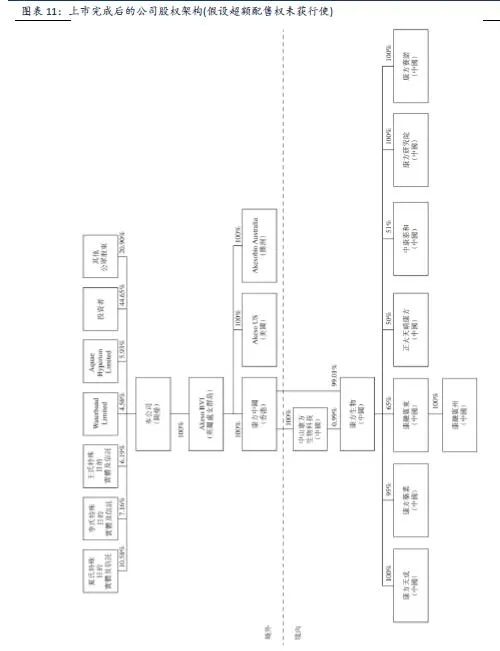
康方生物(09926)是一家临床阶段的生物制药公司,具备国际领先制药公司认可的自主研发能力。致力于自主发现、开发及商业化肿瘤、免疫及其他治疗领域First-in-class和Best-in-class疗法。公司开发出涵盖全面的药物研发和开发功能的端对端平台-康方全方位探索平台(ACE平台),包括靶点验证、抗体药物发现与开发、CMC和符合GMP要求的生产。公司愿景是成为全球领先的下一代创新治疗性抗体企业。
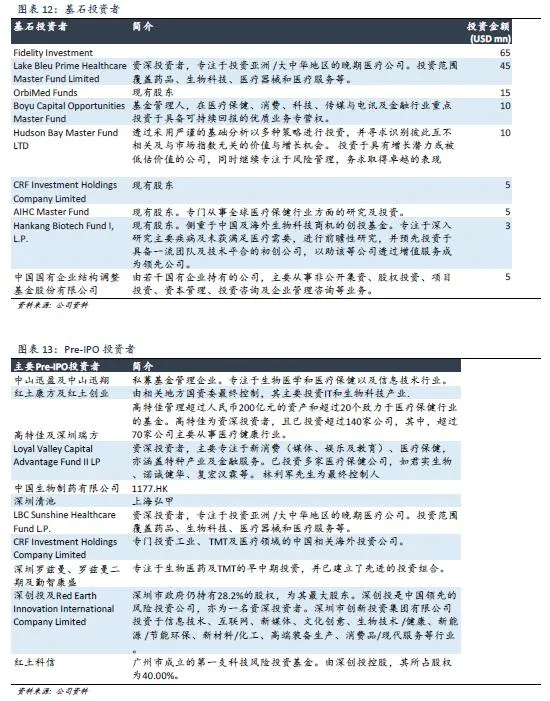
国际领先制药公司认可的研发能力 康方生物是中国首家向全球领先制药公司授权自主研发单抗的生物技术公司。旗下CTLA-4靶点单抗AK107以2亿美元代价授权予默克。此外,公司拥有20多个创新抗体药物管线,包括12个临床阶段抗体,6个双抗(两个处于临床阶段),以及4个获得FDA IND批准的抗体。
潜在的下一代全球首创PD-1/CTLA-4双抗 公司借助专有的四价抗体Tetrabody技术开发出6个双抗产品管线,其中PD-1/CTLA-4双抗AK104和PD-1/VEGF双抗AK112已经进入临床阶段。而主要候选药物AK104已经处于注册性临床试验III期,预计将在2H21在中国首次递交NDA。AK104双抗的初步试验体现出了更好的安全性(较纳武单抗联合伊匹单抗更低的TRAE)和疗效。
PD-1赛道借助中生制药的商业化能力 公司与中生制药(01177)附属正大天晴合作开发和商业化公司的PD-1单抗Penpulimab (AK105),Penpulimab是中生制药唯一的基于PD-1的单一或联合疗法PD-1抗体。借助正大天晴的商业能力,公司PD-1单抗(单用或联合疗法)在拓展适应症、患者入组方面将拥有领先优势。
生产能力 公司中山工厂使用GE Healthcare FlexFactory技术,提供中央控制和一次性生物反应器系统,总产能达到1700升,可以扩大GMP合规生产规模。另外,在建广州生产基地,首阶段计划产能1.6万升,年产能200万个剂量单位,预计于2020年底投入运营。
财务状况 公司目前尚未进入商业化阶段,未有实质收入。2018、2019的研发投入分别为人民币1.6亿元/3.0亿元,净亏损人民币1.4亿元/3.4亿元,经营现金净流出人民币1.2亿元/2.2亿元。截至2019年12月31日,总借贷人民币2.1亿元,现金人民币11.9亿元,总资产人民币16.7亿元。
我们的观点:我们认为双抗较单抗联合疗法拥有更好的安全性和疗效,拥有较大的发展潜力,AK104有望快速商业化。PD-1单抗领域透过与中生制药的合作,差异化竞争,也能够帮助公司在拥挤的赛道中获取更多份额。我们也看好公司受国际领先制药企业认可的研发能力,帮助公司继续推进新药研发、临床试验。
主要风险:1). 在研管线失败 2). 销售推广能力的搭建 3). 优势竞品上市。
公 司 简 介康方生物是一家临床阶段的生物制药公司,是中国首家向全球领先制药公司授权自主研发单抗的生物技术公司。致力于自主发现、开发及商业化肿瘤、免疫及其他治疗领域First-in-class和Best-in-class疗法。愿景是成为全球领先的下一代创新治疗性抗体企业。
肿瘤药物行业全球肿瘤药物快速发展 市场全球肿瘤药物市场属于生物医药市场,专注于发现及商业化治疗癌症的药物。在人均寿命提升,癌症患者人数增加,医疗服务负担能力提高,以及创新和先进疗法的发展的驱动下保持快速发展。根据弗若斯特沙利文的报告,2018年全球肿瘤药物市场规模达到1,281亿美元,预计2018-2023、2023-2030年的复合年均增速分别达到11%和9%。
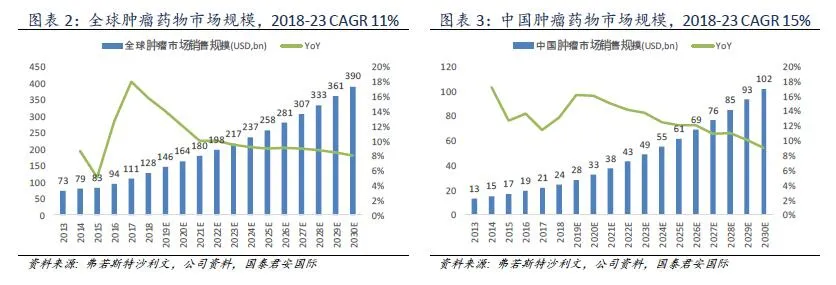
中国肿瘤药物市场增速更高 按销售额计算,中国为全球第二大医药市场。2018年中国肿瘤药物市场规模达到242亿美元,预计2018-2023、2023-2030年的复合年均增速分别达到15%和11%。中国肿瘤药物市场的增速更高于全球市场,主要动力来自于1)庞大且不断扩大的患者人数;2)人均收入增加和医保覆盖扩大,中国医疗支出和负担能力提高。
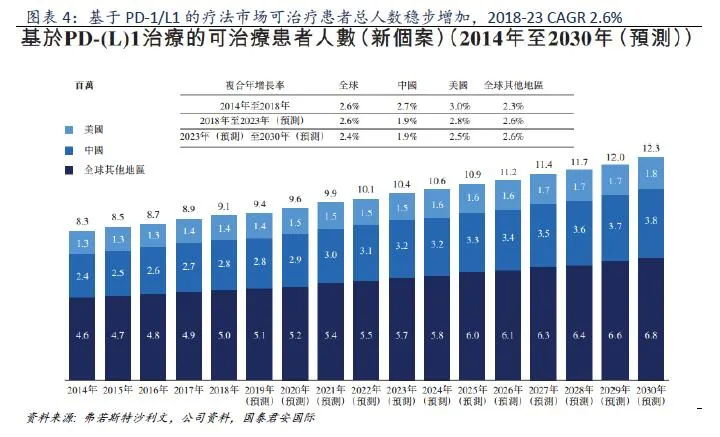
基于PD-1/L1的疗法市场可治疗患者总人数(适应症获批+适应症已在进行临床试验且有望获批的PD-1/L1及CTLA-4抗体的可治疗患者群体)将保持稳步增长。估计2018年中国和美国的可治疗患者总数分别为约2.8百万人及1.4百万人,而2030年则预计会增长至约3.8百万人及1.8百万人。
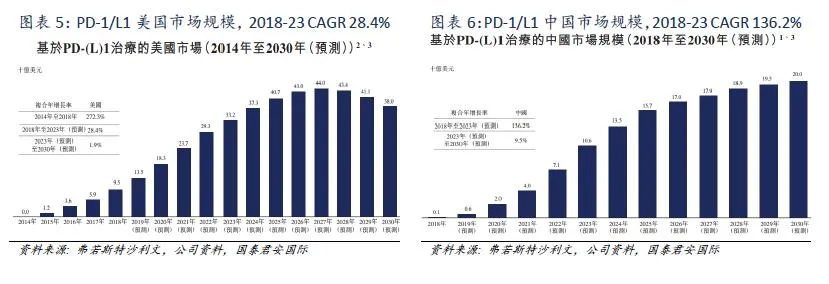
预计2030年中国和美国基于PD-1/L1的疗法市场的市场规模将分别增至200亿美元及380亿美元,其中基于PD-1/L1的双抗疗法预期渗透率将分别达到至少25%及33%。随着更多联合疗法及双抗疗法有望较单一疗法拥有较高的疗效及安全性,这些疗法预期有高参透率及在整个免疫肿瘤治疗市场上取得更大份额。
公司管线自2012年成立以来,康方生物(09926)已开发出中国最丰富及最多样化的抗体药物管线之一,涵盖20多个药物开发项目,包括12个处于临床阶段的开发项目。
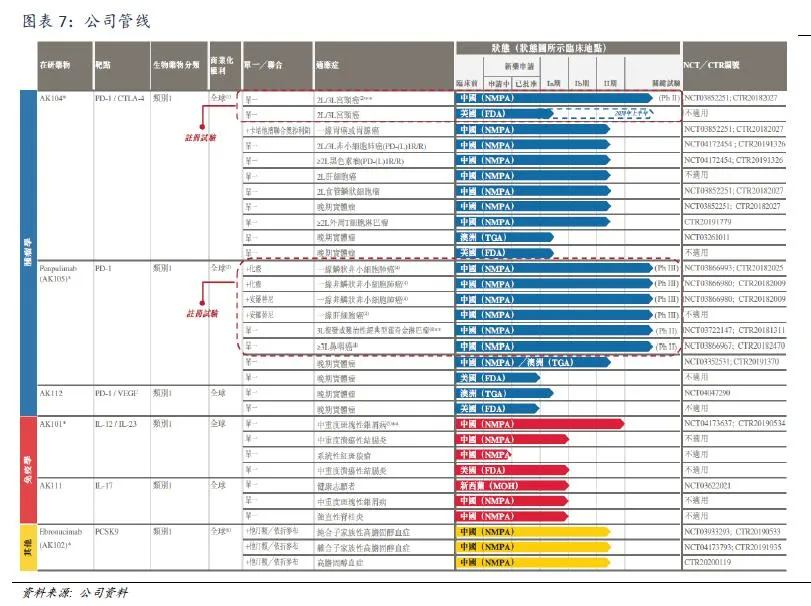

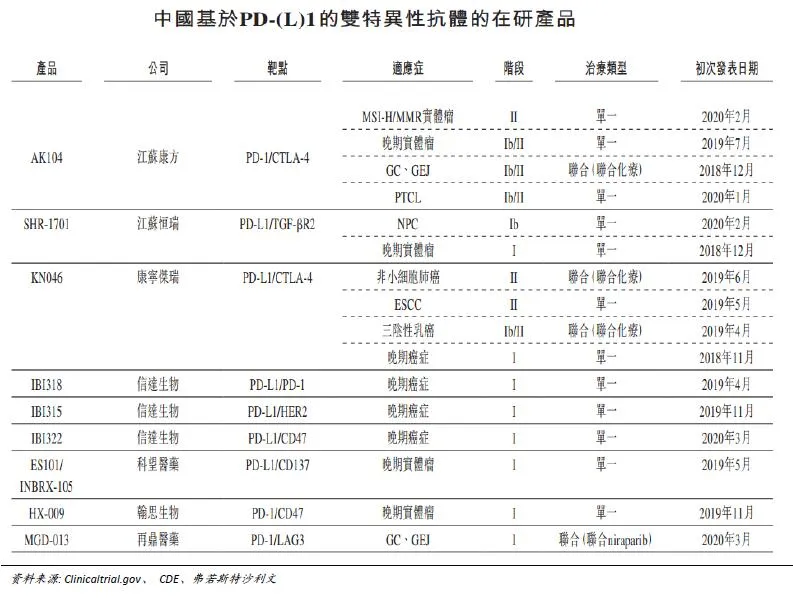
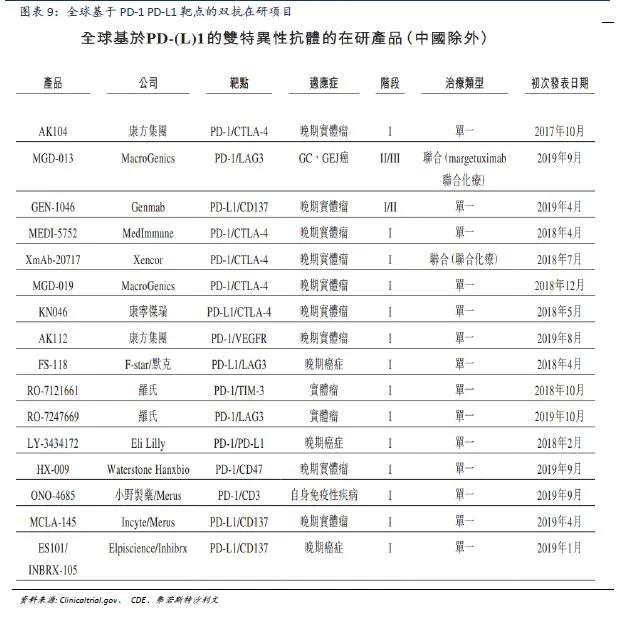
PD-1拥挤赛道中借助中生制药的商业化能力 PD-1/L1赛道已经较为拥挤,中国市场拥有BMS、默克、信达、君实、恒瑞、百济神州等众多产品已经上市的竞争对手。在研产品中也有赛诺菲、复宏翰林、康宁杰瑞等。公司表示Penpulimab (AK105)通过差异化方式(移除不良的可结晶Fc受体介导效用功能),有望成为同类最佳的PD-1单抗。
值得一提的是,Penpulimab (AK105)是中国生物制药唯一可用于开发基于PD-1的单一疗法或联合疗法(如与正大天晴的安罗替尼的联用)的PD-1抗体。我们看好公司通过与拥有中国最大的医药销售团队之一的制药龙头企业中国生物制药的合作。有望借助中生制药的商业化能力(拥有约1.2万人的专业医药销售团队),在拓展适应症、患者入组、商业化推广方面取得优势。
AK105已经在澳洲和中国启动七项临床研究,包括正在中国进行专注于安罗替尼联合试验的五项注册试验。根据目前的临床开发计划,预计将于2020年中在中国提交Penpulimab(AK105)治疗r/r cHL的首次NDA。我们已分别于2018年3月及4月获得FDA针对评估Penpulimab (AK105)的两项IND批准,并计划针对选定的肿瘤类型启动临床试验。
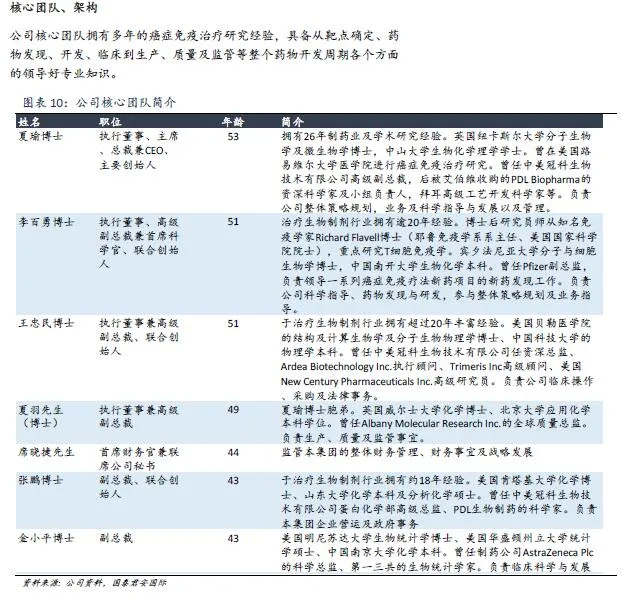
(编辑:李国坚)



 扫码下载智通APP
扫码下载智通APP