新股消息 | 复星系复宏汉霖通过港交所聆讯 已通过自产品销售产生收益
智通财经APP获悉,据港交所8月25日披露,上海复宏汉霖生物技术股份有限公司通过港交所聆讯,中金公司、美银美林、招银国际、复星恒利和花旗担任其联席保荐人,UBS为财务顾问。
2018年4月30日,港交所修订的IPO新规生效,香港正式接纳在收益、市值等方面较为弱势的新经济公司,“允许未有收入或盈利的生物科技公司在港上市”。复宏汉霖作为一家未盈利的生物医药类企业,能赴港IPO正是得益于此项新政。
该公司曾计划在新三板挂牌,当时的申请于2016年12月28日获得受理。但之后,结合复宏汉霖发展需要及各地资本市场特色,董事会于2018年9月27日同意复宏汉霖撤回新三板上市申请,转而投向港交所。
在首次公开发售前,该公司已完成三轮融资,其投资者基础广泛而多元化,包括私募股权及风投基金以及投资控股公司,其中若干专注于医疗行业。除控股股东持有的股份外,就全球发售而言,并无首次公开发售前投资者将须受限于任何禁售安排。
于最后实际可行日期,郭广昌先生持有FIHL约85.29%的股份,而FIHL透过FHL持有复星国际(00656)约70.76%的股份,及复星国际透过其全资附属公司复星高科技间接持有复星医药(02196)已发行总普通股本约37.87%权益,而复星国际由此间接持有复宏汉霖约61.09%已发行股份。
复宏汉霖此番分拆上市后,将继续作为复星国际以及复星医药的间接非全资附属公司;而郭广昌先生、FIHL、FHL、复星国际、复星高科技、复星医药、复星医药产业发展及复星新药将成为其控股股东。合资格复星国际股东及合资格复星医药H股股东将仅有权在分配方面通过优先发售优先参与全球发售。
据悉,复宏汉霖是一家中国领先的生物制药公司,旨在为全球患者提供质高价优的创新药物。该公司是首家根据现行中国有关生物类似药评价及上市审批的法规《生物类似药指导原则》,就单克隆抗体生物类似药自国家药监局取得新药药证申请批准的生物制药公司,也是中国首家商业化推出生物类似药的生物制药公司。
自2010年成立以来,该公司已建立且持续拓展全面的生物类似药及生物创新药产品管线。于最后实际可行日期,除已商业化推出的生物类似药产品(即HLX01汉利康)外,其在管线中自主开发20种以上候选生物药及多种肿瘤免疫联合疗法,其中(i)2种候选单抗获国家药监局接纳新药药证申请,包括1种候选单抗获欧洲药品管理局接纳营销授权申请,(ii)2种候选单抗正在进行3期临床试验及6种候选单抗正在进行1/2期临床试验,以及两种正在进行3期临床试验的肿瘤免疫联合疗法及(iii)已在不同司法权区取得30项新药临床试验申请批准。
复宏汉霖的三处研发中心分别位于上海、台北和加州,于2019年3月31日拥有239名由行业资深人士率领的研发人员。目前已在六个不同司法权区同时进行11项临床试验,并拥有超过100名临床及医学事务人员。其徐汇基地位于上海漕河泾新兴技术开发区,佔地面积约11,000平方米。徐汇基地有6台2000升一次性生物反应器及四台500升一次性生物反应器,拥有总计14000L的产能,规模大且具成本效益。
根据弗若斯特沙利文报告,2020年,该公司三种接近商业化的候选生物类似药连同 HLX01(汉利康)在中国的预计总市场规模将达到人民币167亿元。此外,其部分候选药物获准纳入国家医保目录及国家基本药物目录,这将进一步提高市场渗透率及来自于由中国政府资助的基层医疗基构的需求。
于2017年、2018年及截至2019年3月31日止三个月,复宏汉霖的整体研发开支(包括资本化及费用化研发成本及开支)分别为人民币637.1百万元、人民币972.5百万元及人民币225.4百万元。
下表概述截至最后实际可行日期的产品及候选药物管线:
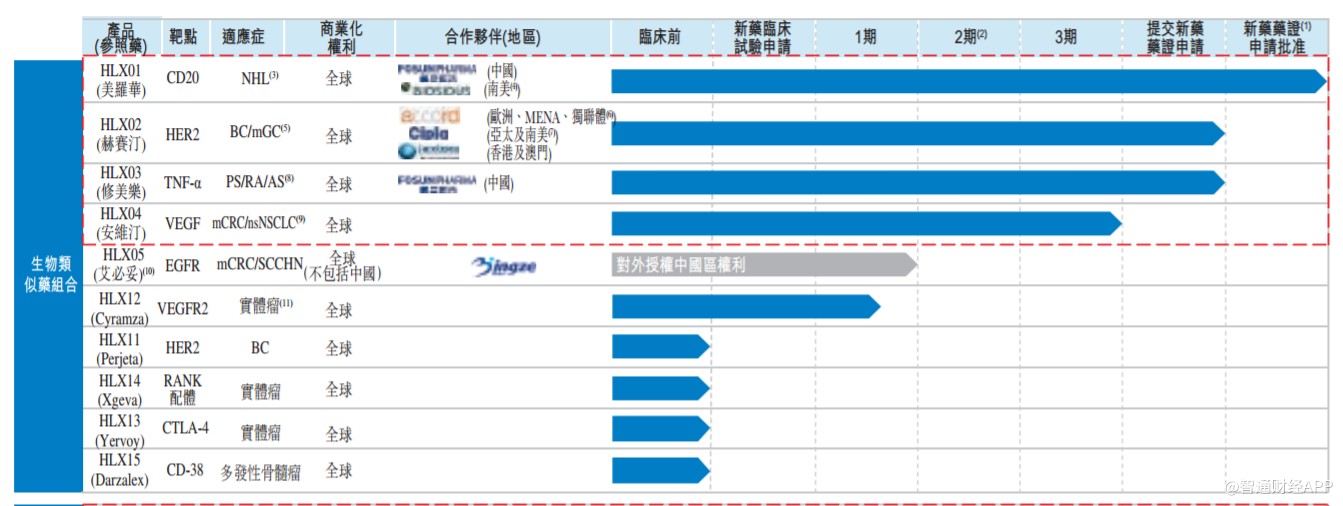

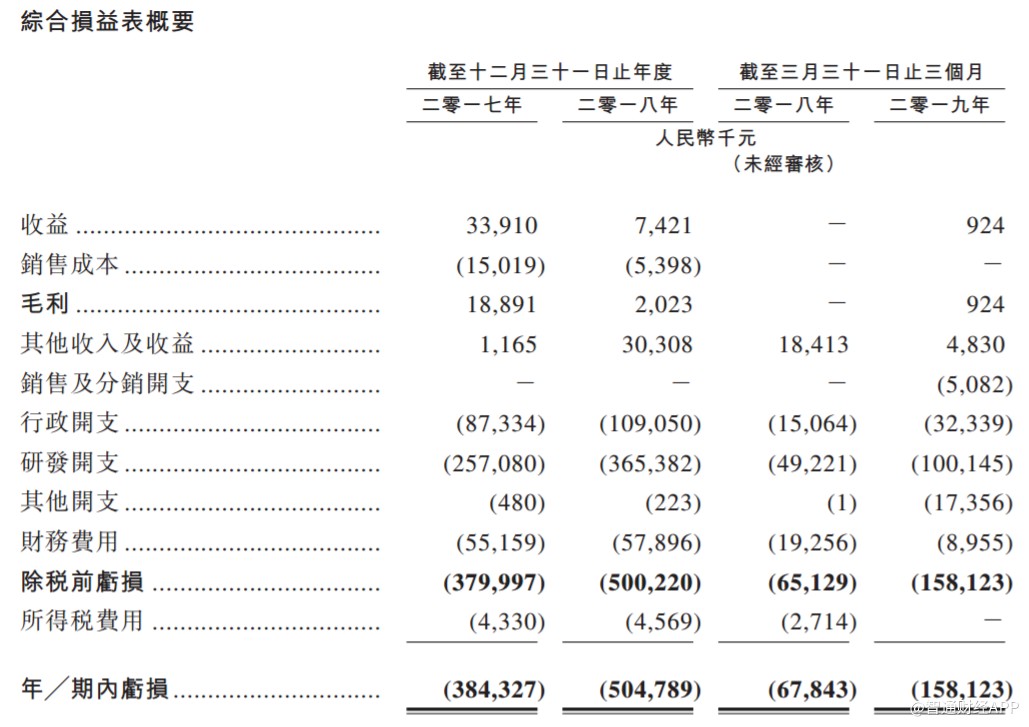
 于往绩记录期,复宏汉霖的收益主要来自许可费收入及向第三方提供服务,且并无通过产品销售产生任何收益。许可费收入的收益主要来自于对上海景泽生物技术有限公司 许可HLX05所收特许授权费。
于往绩记录期,复宏汉霖的收益主要来自许可费收入及向第三方提供服务,且并无通过产品销售产生任何收益。许可费收入的收益主要来自于对上海景泽生物技术有限公司 许可HLX05所收特许授权费。
该公司已改善资产负债表状况,于2019年3月31日实现资产净额人民币1674.8百万元。于2017年、2018年12月31日及2019年3月31日,录得大额无形资产结余分别人民币772.1百万元、人民币1382.6百万元及人民币1507.4百万元,于各该等日期均为资产的最大组成部分。
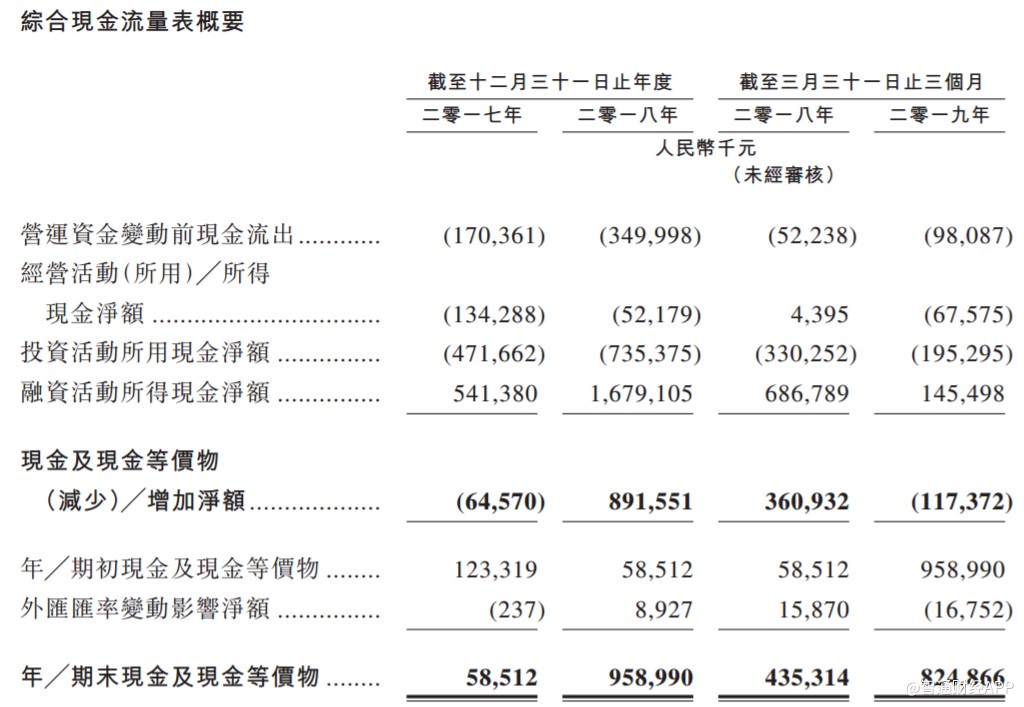 自2019年3月31日起,该公司持续投资及推进候选药物管线的发展,并就商业化HLX01(汉利康)持续开发商业化能力及活动。于最后实际可行日期,其已于徐汇基地开始HLX01(汉利康)的商业生产,并已向商业化合作伙伴交付HLX01 (汉利康)制成品作销售。已于今年四月就HLX02获国家药监局接纳新药药证申请。此外,其商业化合作伙伴Accord于今年六月获欧洲药品管理局接纳营销授权申请。
自2019年3月31日起,该公司持续投资及推进候选药物管线的发展,并就商业化HLX01(汉利康)持续开发商业化能力及活动。于最后实际可行日期,其已于徐汇基地开始HLX01(汉利康)的商业生产,并已向商业化合作伙伴交付HLX01 (汉利康)制成品作销售。已于今年四月就HLX02获国家药监局接纳新药药证申请。此外,其商业化合作伙伴Accord于今年六月获欧洲药品管理局接纳营销授权申请。
由于已在获得新药药证申请批准后开始HLX01(汉利康)的商业化过程,复宏汉霖于截至2019年12月31日止年度及其后的业务性质及获利模型将与往绩记录期大不相同。特别是该公司开始自产品销售产生收益,不同于此前于往绩记录期的收益产生活动主要限于许可费收入及提供服务。但随着推进产品组合及拓展研发管线,其研发开支也会继续产生,将持续对该公司截至2019年12月31日止年度的预期亏损净额造成不利影响。
复宏汉霖拟将IPO所筹资金用于以下途径:1. 用于拨付持续进行的核心产品的临床试验、监管备案及注册;2. 将用于拨付持续进行的候选生物类似药(包括HLX12、HLX11及HLX14)的临床试验、监管备案及注册;3. 将用于拨付持续进行的生物创新药的临床试验、监管备案及注册以及开发肿瘤免疫联合疗法;4. 分配至营运资金及一般企业用途。
于往绩绩记录期,该公司并无宣派或派付任何股息,且并无固定股息派付率。董事会可全权酌情决定是否就任何年度宣派任何股息及(倘其决定宣派股息)宣派的股息金额。
值得注意的是,该公司的业务承受一定风险,投资股份亦存在不确定因素。
复宏汉霖自成立以来已于各期间产生大量亏损,且预期日后将继续产生亏损,并可能一直无法盈利或保持盈利能力,投资者或面临H股投资大幅亏损的风险。该公司于整个往绩记录期的经营活动现金流量为负,且药物开发计划及商业化工作很可能需要额外大量资金,而有关资金未必可按可接受条款取得,甚至可能根本无法取得。仅于近期开始候选药物的商业化,可能难以评估我们的未来前景;加上临床开发过程漫长且耗资不菲,且无法保证结果。



 扫码下载智通APP
扫码下载智通APP