新股研报| 华领医药:糖尿病创新药物的新兴开发平台
本文来自兴业证券的研报《华领医药:糖尿病创新药物的新兴开发平台》,分析师为张忆东、蔡莹琛。
糖尿病创新药物的开发平台:华领医药是一家中国药物开发公司,目前致力于开发用于治疗2型糖尿病的全球首创新药口服药物Dorzagliatin或HMS5552。公司采用VC(资本)+IP(技术)+CRO”的VIC运营模式进行药物开发,一流的研发团队对项目筛选、运营管理和临床实践进行质量控制和监管。目前的产品管线有两款在研产品GKA药物Dorzagliatin与mGLUR5,分别用于治疗2型糖尿病与柏金逊病左旋多巴诱导的运动障碍。
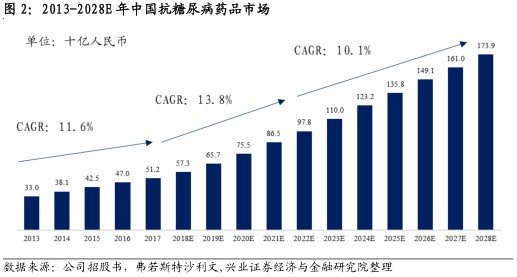
传统药物占据市场主导,创新药物渗透率待提升。中国抗糖尿病药物市场预计将从2017年的人民币512亿元增加到2022年的人民币978亿元,复合年增长率为13.8%。除了胰岛素外,中国抗糖尿病药市场以α-葡萄糖甘酶抑制剂及双胍类二甲双胍等传统药物为主,DPP-4、GLP-1及SGLT-2抑制剂等创新药物的销售收入较少。目前有针对8类靶点超过20款药物在研,创新药渗透率预计会不断提升。
GKA药物III期临床首获批,有望2020年上市。Dorzagliatin具有两大优势:(1)疗效优于现有的口服药。Dorzagliatin临床II期数据优于现有最佳口服药sitagliptin。(2)安全性上克服了以往GKA药物的副作用。由于在临床试验中表现出了良好的耐受性和低副作用,Dorzagliatin是首个进入临床III期的GKA药物,有望于2020年上市,成为未来中国2型糖尿病治疗的一线标准疗法。
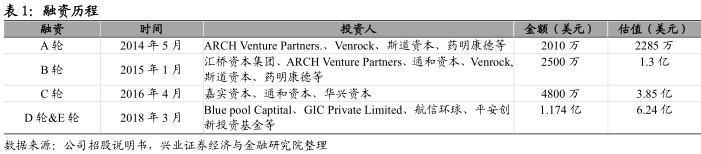
全球知名创投持续看好,5年融资超2亿美金。公司获多家全球知名创投持续看好,总计获得约2亿美金投资。2018年3月27日完成1.174亿美元的D轮和E轮融资。公司股权结构分散,持股比例最高为专注投资早期生命科技公司的ARCHVenturePartners,美国著名风投基金Venrock,富达集团下属斯道资本以及F-Prime基金,分别持有15.07%,12.46%,6.74%、6.23%的股份。此外,药明康德创始人李革夫妇以及李革持30%的WuxiHealthcareVentures分别持有3.37%和8.92%。公司创始人陈力博士家族持有4.95%。
公司简介:糖尿病创新药物的开发平台
华领医药是一家中国药物开发公司,目前致力于开发用于治疗2型糖尿病的全球首创新药口服药物Dorzagliatin或HMS5552。公司于2009年注册成立,2010年罗氏中国研发中心首席科学官陈力博士加入公司。2011年12月公司获罗氏授权开发Dorzagliatin。
全球知名创投持续看好,5年融资超2亿美金
成立以来,公司获得多家全球知名创投持续看好,2018年3月27日完成1.174亿美元的D轮和E轮融资,总计获得约2亿美金投资。目前,公司股权结构分散。持股比例最高为专注投资早期生命科技公司的ARCHVenturePartners,美国著名风投基金Venrock,富达集团下属斯道资本以及F-Prime基金,分别持有15.07%,12.46%,6.74%、6.23%的股份。此外,药明康德创始人李革夫妇以及李革持30%的WuxiHealthcareVentures分别持有3.37%和8.92%。公司创始人陈力博士家族持有4.95%。


VIC模式联合研发,降低药物开发风险
华领医药采用“VC(资本)+IP(技术)+CRO”的VIC运营模式进行药物开发。华领医药引入资本,在全球范围内引进平台与技术,由CRO、SMO及CMO进行产品开发。公司核心团队对项目筛选、运营管理和临床实践进行质量控制和监管,最大程度降低药物研发风险。目前有11家供应商为公司提供临床试验管理、药物制造和分析支持等服务。五大供货商中的其中三名为药明康德新药开发股份有限公司的附属公司。
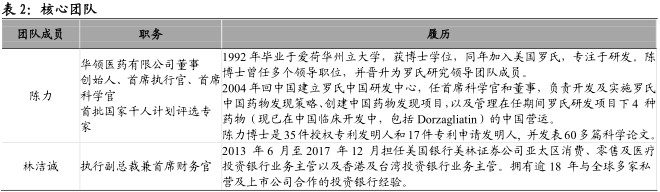
核心团队经验丰富,高管均具有大型药企工作背景。公司创始人陈力博士亦为公司首席执行官、首席科学官,是首批国家“千人计划”评选专家之一,在生物制药行业拥有逾20年经验。加入华领前,陈博士是中国上海的罗氏中国研发中心的创办董事兼首席科学官,一直积极参与Dorzagliatin(现为第四代)的开发工作。加入华领后,陈力博士组建了具有丰富药品研发、管理和运营经验的团队,核心研发团队成员均具有在罗氏、葛兰素史克、辉瑞等跨国药企的工作经验。此外,FranzMatschinsky博士(在发现GK于葡萄糖稳态平衡的中心角色中起作用)担任公司的高级顾问。

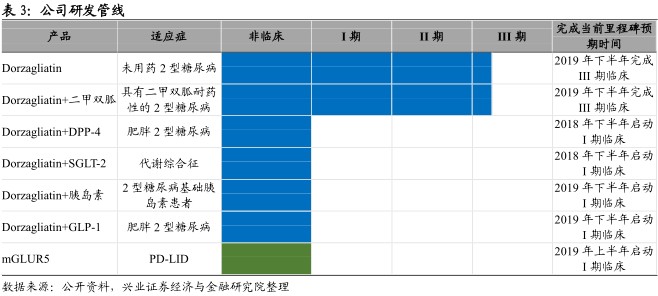
研发管线:主打糖尿病GKA药物及其联合疗法
品公司目前有两款在研产品Dorzagliatin与与mGLUR5。Dorzagliatin是一种葡萄糖激酶激活剂(GKA),旨在通过恢复2型糖尿病患者的葡萄糖稳态平衡来控制糖尿病的渐进性退行性特性。Dorzagliatin作为单药疗法和与二甲双胍联用的疗法目前进行到III期临床。研发管线还包括Dorzagliatin与其它获批的2型糖尿病治疗的的联合疗法,计划在2018和2019年开展临床试验。
另一款在研产品mGLUR5用于治疗柏金逊病左旋多巴诱导的运动障碍(PD-LID),计划在2019年上半年启动I期临床试验。
行业概况:创新药渗透率待提升,多款创新药物在研
受益多重利好因素,2型糖尿病药物市场前景广阔。据弗若斯特沙利文数据,2017年全球约有4.53亿人患有糖尿病,其中4.35亿为2型糖尿病患者,中国是2型糖尿病患者最多的国家,2017年有1.2亿患者。2017年全球抗糖尿病药物市场为689亿美元,预计2022年增加至907亿美元,复合增长率5.6%。随着患者人口增加,慢性病利好政策出台以及创新药物出现,2型糖尿病药物市场呈现利好趋势。中国抗糖尿病药物市场预计将从2017年的人民币512亿元增加到2022年的人民币978亿元,复合年增长率为13.8%。
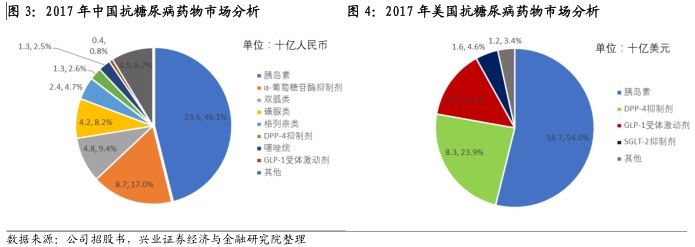
传统药物占据市场主导,创新药物渗透率待提升。中国市场的抗糖尿病药以传统药物为主,而DPP-4、GLP-1及SGLT-2抑制剂等创新药物的销售收入较少。除了胰岛素外,α-葡萄糖甘酶抑制剂及双胍类二甲双胍亦因其价格相宜、降糖效果显着、具有降低心血管疾病风险等其他临床效益而在中国占有重大市场份额。美国则以DPP-4、GLP-1及SGLT-2抑制剂等创新药物为主要药物。
行业竞争激烈,多款2型糖尿病创新药物在研
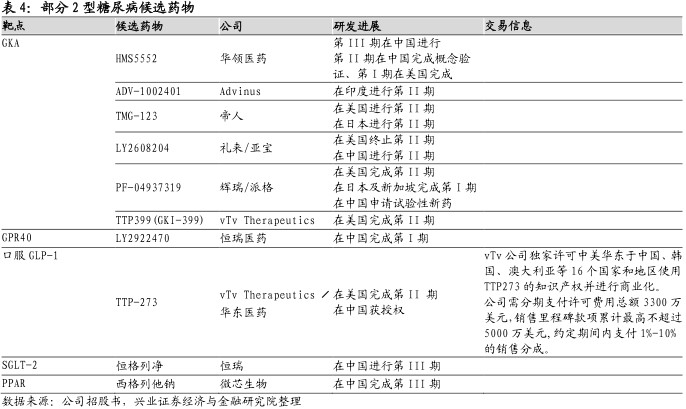
Dorzagliatin面临着既有药物和在研创新药物的激烈竞争。二甲双胍作为主流的治疗药物,通常具有良好的耐受性、已使用超过60年以上且价格相对便宜。创新药物目前有针对8类靶点超过20款药物在研。恒瑞医药的SGLT-2产品进入临床III期,微芯医药的PPAR产品完成临床III期。GKA药物方面,苏州派格于2016年从辉瑞获得了GK化合物许可,但尚未在中国启动临床试验。亚宝从EliLilly获得了GK化合物许可,正在中国进行其GK化合物的I期试验。于中国以外,帝人、VTV也在不断推进其GKA。
产品优势:疗效与安全性双加持,GKA药物III期临床首获批
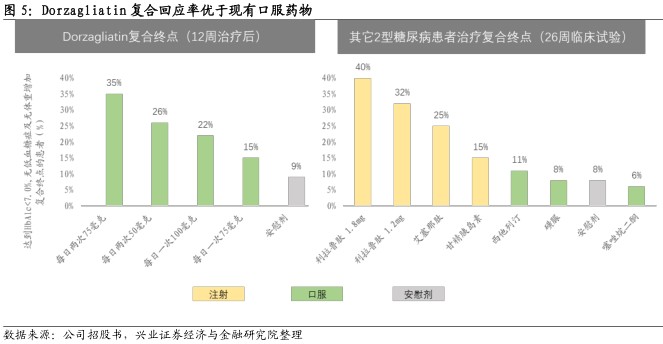
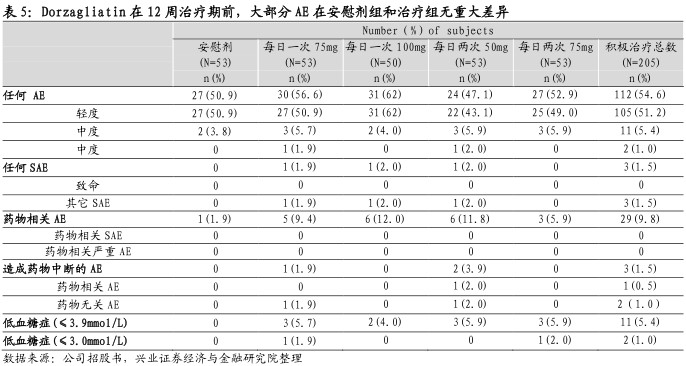
Dorzagliatin具有两大优势:(1)疗效优于现有的口服药。目前批淮的2型糖尿病药物侧重降低血糖水平,但未能阻止负责制造胰岛素的β细胞功能恶化的问题,从而无法维持葡萄糖稳态平衡。GK在葡萄糖稳态中发挥的作用在二十多年前被揭示,是糖尿病理想的治疗途径。Dorzagliatin在临床II期12周试验中,35.4%的患者达到了复合终点,包括HbA1c水平血糖控制至7%以下,且未出现体重增加及低血糖情况。之前表现最佳的口服药是sitagliptin(口服DPP-4抑制剂及全球最畅销的口服抗糖尿病药),仅11%患者使用后到达该等复合终点。
(2)安全性高于以往GKA药物。以往GKA药物由于化学结构相关的缺陷引致疗效不足、低血糖风险增加、血脂异常及肝脏中毒等多种问题而未能完成临床II试验。Dorzagliatin由于采用独特的化学结构并通过双重作用机制在I期及II期临床试验展现了良好的耐受性和低副作用,成为首个成功进入临床III期GKA药品。
2020年有望上市,具备成为中国2型糖尿病一线疗法潜力。Dorzagliatin在中国的III期临床试验预计在2018年下半年完成患者入组,并在2019年下半年公布试验结果。在获得正面的结果后,计划在中国提交作为一类新药的新药申请,并在2020年之前取得或国家药监局的新药上市批准。公司认为Dorzagliatin有望在该种进展性疾病的各个阶段推进2型糖尿病的治疗标准,解决糖尿病治疗中普遍未满足的医疗需要,成为中国2型糖尿病治疗的一线标准疗法。
资金用途
筹集的资金主要用于Dorzagliatin的后期研发和商业化。

财务分析
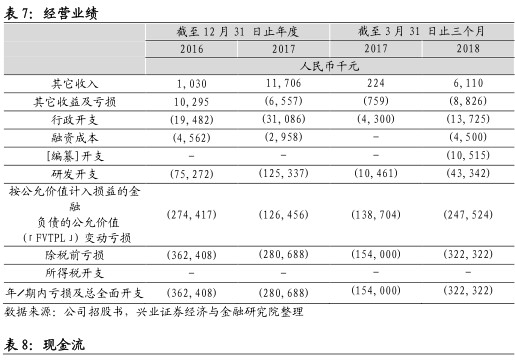
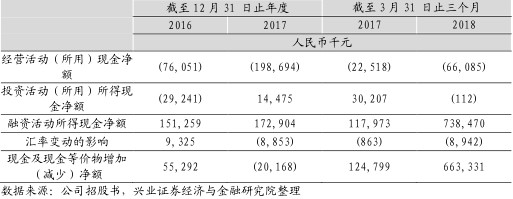
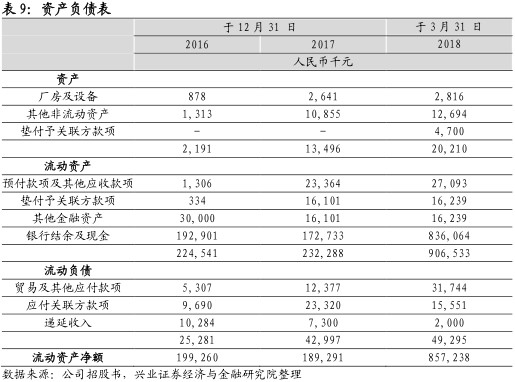
公司合计亏损近10亿,现金流较为充足。华领医药尚未有产品实现商业化,迄今未通过销售商品产生收益,仅以政府补贴及银行利息确认有限收入,分别在2016年、2017年和2018年3月31日截止前确认60万元,1050万元和580万人民币的政府补助。2016年-2018年Q1分别亏损3.6亿、2.8亿和3.22亿,累计亏损近10亿,主要由于研发开支和按公允价值计入损益的金融负债的公允价值变动亏损造成的。截止2018年3月31日,公司拥有8.36亿银行结余与现金。
风险提示
与有限的经营历史、过往亏损及对关键执行人员的依赖有关的风险:公司经营历史有限且过往出现亏损,须取得必要监管批准后方可推出Dorzagliatin及产生收益;可能无法挽留关键管理人员及吸引、挽留和激励有资质的人才。
与在中国成功开发、获取监管批准及商业化Dorzagliatin有关的风险:Dorzagliatin第III期临床试验可能延误或失败,商业化可能严重推迟或失败;第三方机构依赖性风险;联用的任何获批准2型糖尿病可能出现安全、疗效、生产或供应的问题;产品上市后可能不受认可。
与在中国境外批准及商业化Dorzagliatin(包括任何组合药物)有关的风险:取得境外监管批准的额外挑战,寻找国际医药公司及其他合作伙伴可能失败
与知识产权有关的风险:可能无法为Dorzagliatin取得及维持专利保护,或所取得的知识产权保障范围不够广泛,面临第三方的直接竞争等
与业务有关的其他风险:可能在应对增长方面遇到困难,合作伙伴可能从事不当行为等
与在中国经营业务有关的风险:中国政府的政治、经济和其他政策不利变化可能会对中国整体经济增长产生重大不利影响。中国法律、法规或执行政策发生变化,汇率波动风险等(编辑:王梦艳)



 扫码下载智通APP
扫码下载智通APP