医疗新赛道:谁将填补PD-1治疗失败后的头颈鳞癌治疗空白?
自2009年迎来第一次大型药企IPO后,港股医疗健康板块已由当初400亿市值扩容至2021年的超4万亿港元规模,这便是港股18A以来的成果写照。数据背后,则是市场对生物医药如PD-1\PD-L1、免疫治疗、重磅靶向药物等的追捧。
而随着君实、信达、恒瑞、基石等在PD-1\PD-L1的竞赛步入深水区,投资者也逐渐将目光转向更多细分赛道,如重磅靶向新药、差异化治疗等更加创新的标的之上。其中,于近期递表的阿诺医药所正在进行三期临床试验的头颈鳞癌靶向新药AN2025,便是其中之一。
7月23日,在临近世界头颈肿瘤日之际,经美国临床肿瘤学会(ASCO)官方授权举办的2021 ASCO Direct China “头颈癌临床进展”交流会于上海顺利召开。
会议期间,同济大学附属东方医院一期临床试验中心主任、中国临床肿瘤学会头颈肿瘤专委会主委郭晔教授接受智通财经APP专访,详细阐述了我国头颈鳞癌当前最新的临床研究进展及未来发展方向。
何为头颈鳞癌?
智通财经APP了解到,头颈癌为根据解剖部位不同所划分出来的一大类癌症的统称,其原发部位和病理类型众多,主要包括颈部肿瘤、耳鼻喉科肿瘤以及口腔颌面部肿瘤三大部分。
其中,由于头颈癌所包含的大部分器官均与外界相通,该类癌症有超过90%的头颈部肿瘤为鳞状细胞癌,余下10%则为以腮腺、颌下腺、舌下腺、小唾液腺等唾液腺肿瘤为主的唾液腺癌。
郭晔教授向智通财经APP表示,头颈癌的发病率涉及到编码的不同,主要分为唇和口腔、鼻咽和喉咽、喉和下咽三个编码区域。若将三个编码区相加,头颈癌在男性恶性肿瘤发病率中则占第七位,死亡率占到第六位。
其中,因以抽烟酗酒为最主要致病因素,头颈癌为较为重要的男性疾病之一,发病男女比例约8 : 2。同时,我国当前抽烟喝酒人口仍居高不下,因此头颈癌的发病率也尚未出现明显下降趋势。
在我国,头颈癌患者多以有抽烟酗酒习惯的男性为主,普遍为不积极就医的一类人群,就诊往往已处于中晚期,因此疾病预后较差。据郭晔教授介绍,约有一半左右的头颈癌患者会出现复发转移,导致治疗难度大大提升。一般而言,复发转移患者的中位存活期不到十个月,五年存活率约仅为30-40%。
头颈鳞癌PD-1治疗方案前移 二线现亟待填补空白
智通财经APP了解到,传统的头颈鳞癌治疗方案是以先化疗为主,或以化疗联合靶向药进行治疗,药物治疗较为局限。而近年来,头颈鳞癌也和肺癌等其他恶性肿瘤癌一样,以原先作为二线治疗药物的PD-1前移至一线作为一大突破点,治疗疗效进一步提高。
然而,二线药前移也引发另一个新的问题。据郭晔教授表示,随着PD-1的前移,头颈鳞癌在PD-1治疗失败后,二线的标准治疗将处于空白状态,对于二线而言存在未满足的临床需求。阿诺也正是基于这一点,在全球范围内开展PD-1失败后的二线治疗注册性临床试验,寄望以此来改变二线治疗的格局。
有最新研究数据表明,在头颈鳞癌患者中,PD-1一线免疫治疗的四年生存率约在20-25%左右。也就是说,每4-5人中仅有1位患者可存活超过四年;而这20%的患者能否撑过五年或更长时间,还仍需进行更长时间的随访。这也表明,绝大多数头颈鳞癌患者通过免疫治疗是无法解决问题的,二线标准治疗的空白正亟待被填补。
据郭晔教授介绍,除免疫治疗被广泛应用在头颈鳞癌的治疗中外,一些特殊的靶点如细胞周期、PI3K抑制剂等也在近年头颈肿瘤的临床中取得一定突破。其表示,未来化疗虽仍会占有一席之地,但更多的解救治疗还需探索肿瘤本身的信号通路及其与免疫之间的关系,从而发掘更多联合方案实现缓解率改善、延长生存。
据介绍,以临床试验的角度来看,PI3K抑制剂现已有二期的对照研究显示能够改善总生存,为当前最有希望成为二线标准治疗的方案之一,也是当前唯一有随机研究结果的方案;其他新型药物研究如细胞周期,目前所做的仍为一些单臂研究,尚缺乏随机研究的背景。
除此之外,PD-1作为当前标准的一线治疗方案,约有40%的患者可仅采用PD-1而无需进行化疗,另外60%则需化疗与PD-1联用。据郭晔教授介绍,头颈鳞癌当前最新的研究方向之一便是如何将这40%的人群范围扩大,如采用双免疗法,包括默沙东在做的帕博利珠单抗联合仑伐研究等。
另一方面,PI3K中的δ、γ亚基和免疫系统有较大关联性,也有许多研究表明此类抑制剂药物与PD-1会有更好的协同作用。郭晔教授对智通财经APP表示,若PI3K抑制剂将来能够在二线治疗方案中获得成功,其未来自然也有望向一线转移,与PD-1进行联用,从而扩大对免疫和靶向有效的人群范围。但从临床试验的角度都是先从后做起,证明其有效后再逐渐前移。
走在头颈鳞癌临床研究前沿 AN2025有望率先出线
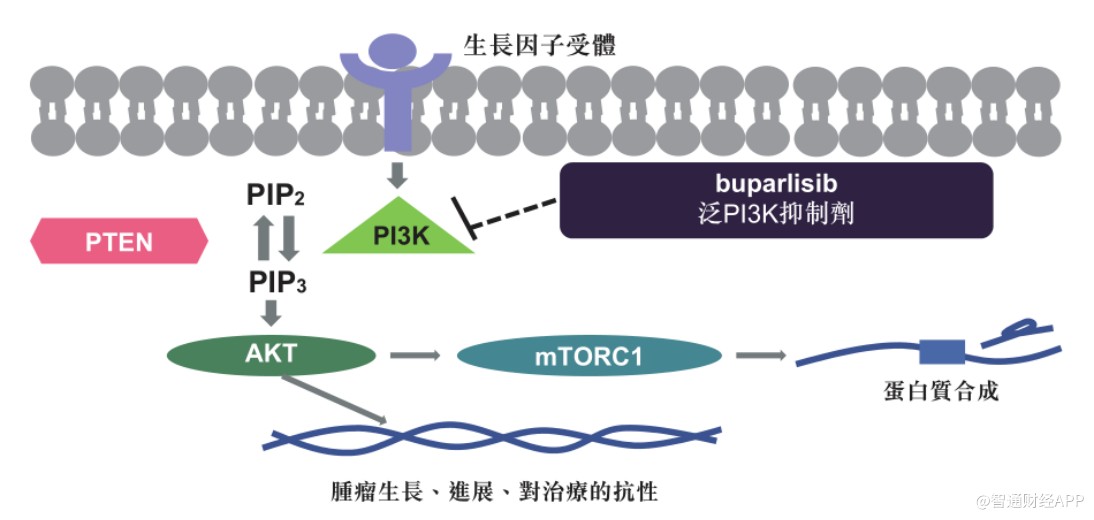
据智通财经APP了解到,PI3K为肿瘤当中较为重要的靶点之一,其代表了一个非常重要的通路——PI3K/AKT/mTOR通路,该通路为许多肿瘤包括乳腺癌、头颈鳞癌重要的肿瘤生长信号通路。在人体中,正常细胞同样依赖该通路,而肿瘤细胞则过度依赖。通路的过度激活将导致肿瘤细胞的快速生长,其中相关抑制剂对肿瘤的生长起到了抑制作用。
在最新的PI3K抑制剂研究中,全球处于临床阶段的泛PI3K抑制剂共有四种;中国处于临床阶段的PI3K抑制剂则有九种。
其中,AN2025 (buparlisib)为所有PI3K抑制剂研究中最先进入临床阶段的泛PI3K抑制剂。据了解,AN2025作为一款泛PI3K抑制剂,其不仅靶向PI3K介导的肿瘤发生(如通过抑制PI3Kα/PIK3CA突变体),同时亦靶向免疫抑制的肿瘤微环境(如通过抑制PI3Kδ及PI3Kγ)。
据郭晔教授向智通财经APP介绍,AN2025的早期研究集中于乳腺癌领域,研发过程中存在的一些不良事件(AE)主要与精神系统相关,患者在用药后会出现一定的抑郁或食欲下降。其中,主要由于乳腺癌多集中于女性患者,相对于男性更易发生精神方面的不良事件。
而在AN2025的目前研究中,精神相关的不良事件在以男性为主导的头颈鳞癌中发生率则较低。相对而言,临床试验的3-4级AE更多发生在血糖代谢方面。
已有许多临床试验证明,PI3K是血糖代谢非常重要的一个通路,大部分患者在使用抑制剂后会出现血糖紊乱,如不及时处理便很容易转为3-4级AE。在临床研究早期,许多研究者对PI3K抑制剂导致高血糖的概念和处理能力尚不成熟。而随着认识的逐渐深入,研究者在用药时配合使用降糖药对血糖进行提前关注,轻度AE便不会发展成严重的AE或SAE。
据智通财经APP了解,AN2025现已完成与紫杉醇联用治疗铂类药物治疗后复发性或转移性头颈鳞癌的多中心II期临床试验,并展现出较好的临床数据表现。其中,将AN2025与紫杉醇联用治疗组相较于安慰剂加紫杉醇组对mOS的提升由6.5个月增至了10.4个月,mPFS也由3.5个月提高至4.6个月。
据研究者评估,AN2025治疗组的客观缓解率(ORR)较安慰剂组提高约3倍(39.2%与13.9%),服用AN2025的患者亦保持稳定的生活质量,显示出对治疗的良好耐受性。
目前,AN2025正在开展样本更大的随机三期研究。据了解,该研究预期在全球约150个站点招募480余名患者,涵盖北美洲、欧洲及亚洲共超过15个重要市场;并预期于2023年下半年利用III期中期分析数据提交,以快速审评通道向FDA提交NDA申请,随后将向国家药监局、EMA、PMDA及其他机关提交更多NDA申请。
对于AN2025的前景展望,郭晔教授表示,AN2025为目前头颈鳞癌临床研究中走在前沿的药物。此外,其在头颈鳞癌未来与多款药物的联用方面也展现出了较好的基础,例如除与化疗联用外,AN2025还具备与PD-1及其他抗EGFR靶向药联用的基础。目前,头颈鳞癌领域中还没有针对PD-1失败进行注册研究的药物,若AN2025三期临床试验能够重复二期的研究结果,其将有望快速填补PD-1治疗失败后二线标准治疗的空白。



 扫码下载智通APP
扫码下载智通APP