V-01新冠疫苗迅速推至II期临床,丽珠医药(01513)的重组蛋白路线有哪些期待?
虽然全球获批使用的新冠疫苗不断增加,但这场疫情仍未到达人类最终胜利的拐点。新冠疫苗接种率超过60%的塞舌尔近期出现了新一轮病毒传播,4月里,印度单日确诊病例数更是从10万人迅速攀升至40万人。
一方面,新冠病毒突变株威胁着既有疫苗的有效率。《新英格兰医学杂志》刊登的一篇论文指出,B.1.351突变株对康复者血清和新冠灭活疫苗接种者血清具有较强的逃逸能力。
另一方面,产能不足制约了全球范围内的疫苗公平分配,而血小板减少性紫癜、凝血等mRNA、腺病毒载体产品带来的不良反应,也一定程度地加剧公众的“疫苗犹豫”。因此,持续评估疫苗对突变株的保护效力,开发出多种技术路线的新型疫苗仍十分必要。
重组蛋白新冠疫苗一直都是行业关注的重点方向之一。今年3月,智飞生物采用工程化细胞(CHO)生产的重组蛋白疫苗成为国际上首款获批临床使用的产品。而从临床的推进和佐剂的设计上,丽珠集团(01513,000513.SZ)控股子公司丽珠生物的表现有望“更上一层楼”。
去年7月,丽珠生物全资子公司丽珠单抗与中科院生物物理研究所联合研发的重组新冠病毒融合蛋白疫苗(项目代码:V-01)正式立项。从时间上看,现阶段即将完成II期临床。
V-01自今年获批开展临床试验后,迅速对产品的安全性、免疫原性展开验证。援引中国临床试验注册中心披露的信息,4月7日,丽珠单抗更新了I、II期临床的资料。I期临床所采用的剂量爬坡设计,包含10μg、25μg和50μg三个剂量组,入组180例18岁及以上健康受试者。其中,成人组90例,每个剂量组30例;老年组90例,每个剂量组30例。

丽珠单抗V-01项目I期临床注册信息
设计上,V-01创新性地融合了作为生物佐剂的人源细胞因子等免疫活性成分,以新冠病毒刺突糖蛋白(S蛋白)的受体结合区(RBD)作为抗原,采用Fc融合蛋白设计而成,以全面、长效激活抗新冠病毒的免疫应答。
这种策略对丽珠生物而言显得驾轻就熟。早在去年,丽珠生物就将类似的探索推至临床。当时的公告透露,丽珠单抗通过IgG的Fc片段与活性蛋白连接构成融合蛋白,延长了抗肿瘤创新药物A-01的半衰期。
基于已有资料和数据,仅使用RBD的疫苗难以触发强大和持久的免疫反应。为了增强淋巴结对抗原的加工和交叉表达,提高RBD的免疫原性,丽珠单抗开发了第二代融合蛋白疫苗,即干扰素修饰的RBD二聚体(I-R-F)。I-R-F在N端携带干扰素α,C端与人IgG1 Fc形成二聚体,用于靶向淋巴结中的树突状细胞,通过干扰素和Fc二聚体去增强抗原加工和呈递。
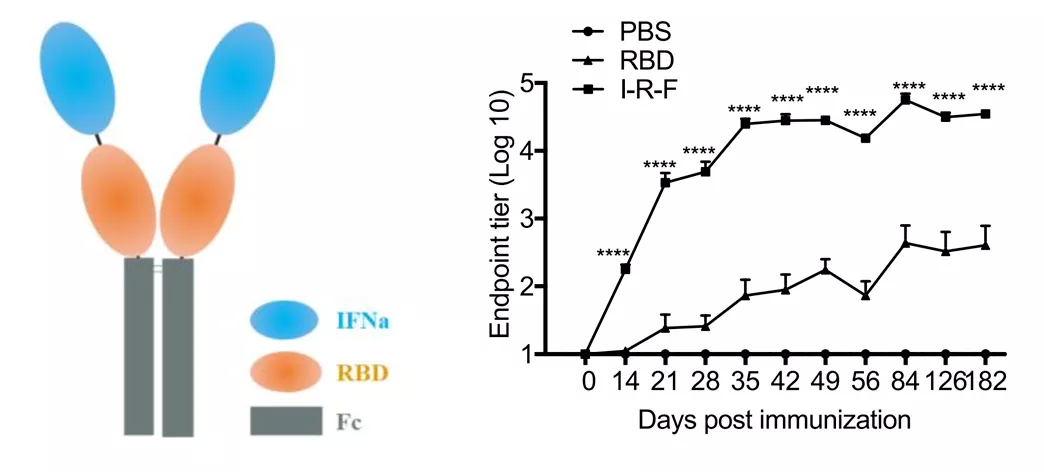
I-R-F结构及其在小鼠模型诱导的抗体应答
实验证明,低剂量(0.01 ug)的I-R-F甚至没有佐剂的情况下,V-01都可以在小鼠体内诱导高滴度、持久的中和抗体,同时能激活全面的细胞免疫。恒河猴攻毒试验中,高剂量SARS-CoV-2组中I-R-F也提供了快速和全面的上、下呼吸道的保护。
通常,佐剂很大程度上决定传统疫苗的效力和安全性。当前行业最常使用的佐剂是铝盐,例如磷酸铝、氢氧化铝。这类佐剂的缺陷在于激发细胞免疫不足,可以减少新冠病毒抗原的用量、提升疫苗免疫效果的新型佐剂,成为免疫学界的课题方向之一。
不过这也并非万全之策。佐剂可能带来一定的副作用,尤其是新型研发的佐剂,生产成本高昂,常见不良反应发生率常高于氢氧化铝佐剂。在Novavax加入Matrix-M佐剂的重组蛋白新冠疫苗I、II期临床试验中,接种后的局部疼痛率超过40%、疲惫率超过40%,全身肌痛率超过30%,感觉不适率超过28%。
从这一点来说,如何找到佐剂作用的平衡,也是布局重组蛋白等技术路线的药企们亟需重视的方面。
理想的新冠疫苗应具有以下特性:一是具有高滴度的中和抗体和足够的安全性,二是能够延长保护性免疫力,三是方便大规模生产存储和分配。
丽珠生物的策略,不仅绕开了新型佐剂的生产和安全性问题,同时最大限度地减少对佐剂的依赖。V-01加入较为常见的明矾佐剂,降低严重毒性发生概率的同时,使I-R-F分子缓慢释放到引流淋巴结(DLN)中。
一篇发布于bioRxiv的论文指出,丽珠生物设计了一种即使在极小剂量,或者没有佐剂的情况下也具有极强免疫原性的I-R-F疫苗V-01,有望为预防新冠病毒提供更加高效的方法。
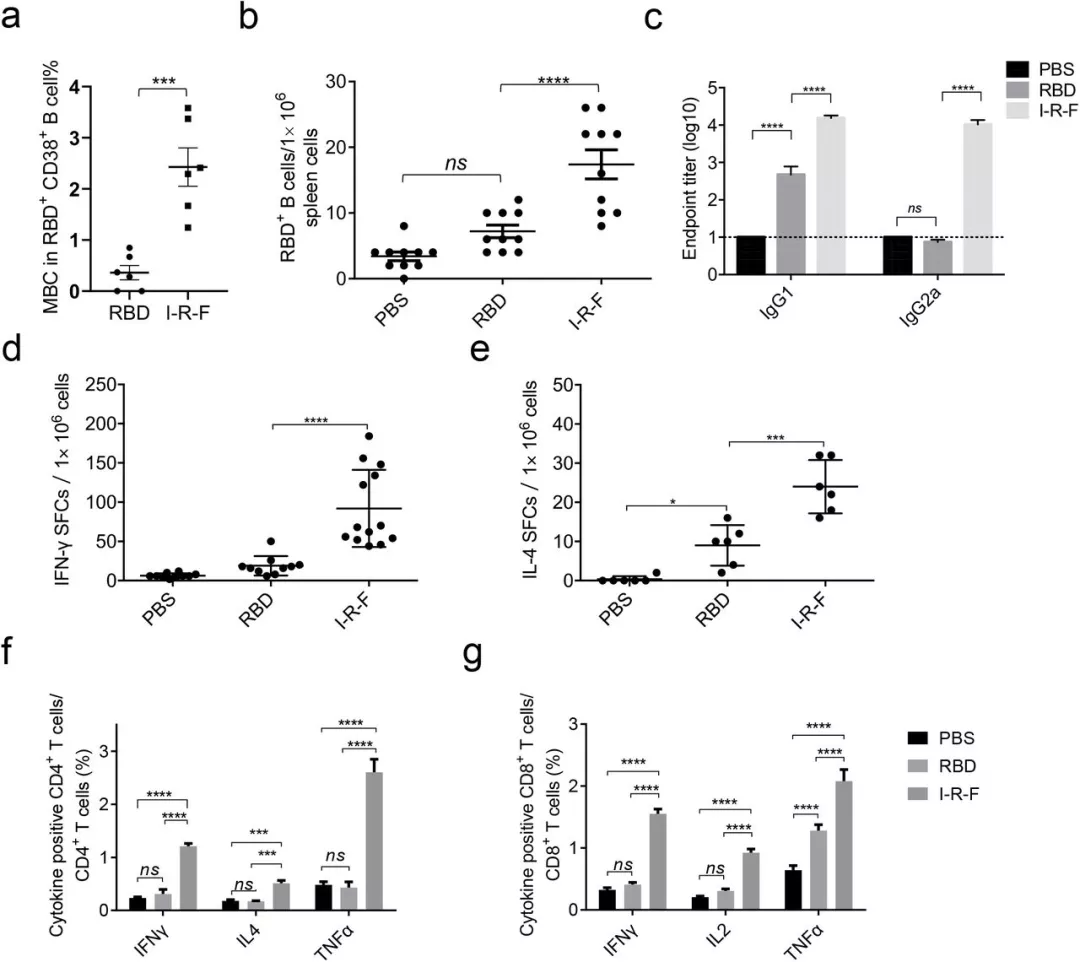
IRF诱导SARS-CoV-2特异性Th1、Th2和CD8+T细胞免疫反应
依照丽珠生物全资子公司丽珠单抗和中科院生物物理研究所的合作分工,经后者开展新冠病毒融合蛋白疫苗的前期研发,在基础研究和前期实验动物模型取得重大突破后,由丽珠单抗负责工程细胞株的构建、生产工艺开发、临床前药理毒理研究、注册审批、临床研究及商业化生产及全球推广等工作。
据悉,随着I、II期临床的顺利开展,丽珠生物正在准备下一阶段的试验。针对突变株问题,丽珠生物在V-01之外还布局了相应的管线,目前正在稳步推进研发工作。
与此同时,为了尽早满足全球对于新冠疫苗的需求,丽珠生物基于多年研发抗体药物、重组蛋白等大分子类生物制品的经验与优势,已推进疫苗商业化生产车间建设优化等工作,为疫苗的早日上市创造条件。
本文选编自微信公众号“同写意”;智通财经编辑:曾盈颖。



 扫码下载智通APP
扫码下载智通APP