“医药论坛”实录丨永泰生物-B(06978): 国内首款实体瘤细胞免疫治疗产品,2020年年底将全部入组完毕,2021年上半年进行中期数据分析
11月13日,由港美股资讯第一平台智通财经与大湾汇联合主办、专业财经路演直播平台“大路演”提供全程路演支持的“2020智通财经&大湾汇医药投资论坛”于上海隆重启幕。
在“2020智通财经&大湾汇医药投资论坛”上,永泰生物-B(06978)CFO杨宁就公司发展现状、战略,与现场投资者做了零距离的面对面沟通。

永泰生物是第一家根据香港联交所《上市规则》第18A章申请上市、核心产品为细胞免疫治疗产品的公司。公司的核心产品为“扩增活化的淋巴细胞(EAL)”。EAL是中国首款、也是目前为止唯一一款进入II期临床试验、适应症为实体瘤(肝癌)的细胞免疫治疗产品。
除核心产品EAL之外,公司在CAR-T的管线也有重要布局。CAR-T和EAL同属于细胞免疫治疗产品里面的不同的分支。EAL是非基因修饰、多靶点的细胞免疫治疗产品;而CAR-T是以基因修饰为基础的靶向治疗。
永泰生物的主要研发管线如下:
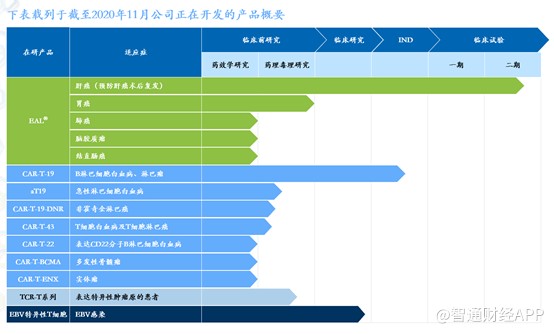
关于EAL:
在EAL肝癌适应症方面,永泰生物于2015年8月提交了临床试验申请,2017年10月获得IND批件,2018年9月入组了第一例病例。目前,相关的临床试验进展顺利,临床试验中心为中国人民解放军总医院(301)、北京协和医院等国内14家顶级三甲医院。该临床试验截至目前已经入组了236例病例,预计将在2020年年底前入组完全部272例病例。在II期临床试验得出有统计学意义的中期数据之后,永泰生物将向药监局提交药品有条件上市申请。根据目前临床试验的进展,中期数据分析将在2021年上半年完成。除手术外,肝癌目前没有太好的治疗手段,因此永泰生物的EAL在肝癌治疗领域具有强劲的先发优势。
在EAL扩大适应症方面,永泰生物正在开展胃癌、肺癌、结直肠癌和脑胶质瘤的临床前研究,并预计将在2021年提交胃癌适应症的临床试验申请。在2006年至2016年期间,永泰生物积累了10年EAL产品的临床应用经验,其中胃癌的病例数为270例病例、1350次回输。
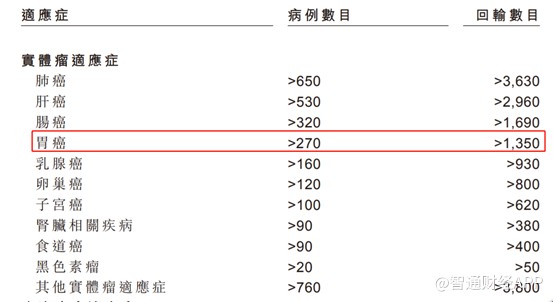
在2015年中国人民解放军总医院张国庆主任发表的回顾性临床研究中,EAL产品在延长胃癌患者总生存期方面,具有显著的统计学意义差异:其中试验组的总生存期为27个月,而对照组为13.9个月,P值为0.028(P值小于0.05即为具有显著的统计学意义差异)。
其他管线:CAR-T-19预计今年可以进入I期临床;aT-19和CAR-T-19-DNR明年可以申请临床并开始试验。
商业化:永泰生物在北京已经取得了50亩地用于细胞免疫治疗产品的研发及商业化。北京的细胞制备中心预计在2020年年底前开工建设,明年年底一期完工并完成GMP生产认证,以匹配EAL的商业化进度。受EAL运输半径的限制,永泰生物将在全国6-7个城市建立细胞制备中心,其中上海和广州的相关工作已经启动。
财务数据:永泰生物目前还处于研发阶段,预计最晚于2022年产生收入。根据预测,永泰生物将在EAL产品商业化当年进入盈利状态。
以下是智通财经APP整理的永泰生物现场会议问答实录:
Q1:EAL从自体血采集到制备的时间周期?
A1:EAL在自体血采集之后,根据患者体质的不同,需要在体外做12-17天的制备。
Q2:我理解目前EAL还是需要配合手术使用,请问是这样么?
A2:在目前癌症还是“不治之症”的情况下,EAL产品和手术的关系不应该说成是有主次的“配合”关系,而是多种疗法联合治疗。EAL产品和包括手术在内的其他治疗手段在癌症的治疗过程中是互补的关系:手术快速清除影像学可见的肿瘤;而EAL产品清除肉眼看不见的、残存散状癌细胞,预防术后复发。此外,EAL产品与化疗、PD-1抗体等联合使用,都会达到“1+1大于2”的效果。
Q3:后面的回输频次大概多久?如何定价?
A3:根据目前肝癌的临床试验方案,使用EAL产品进行治疗,一年须做20次回输。定价目前还没有确定,预计将会参考日韩同类产品而确定。目前在韩国同类产品一次回输价格为美元5,000元。



 扫码下载智通APP
扫码下载智通APP