自研抗体及技术平台入选NASH-TAG大会,来凯医药-B (02105)差异化创新平台有望实现肝纤维化治疗突破
通常来说,创新药物的研发和审评是以临床价值为导向,而创新生物药企的内在价值也需要可靠的研发成果来印证。
所以在港股18A公司中,有这么一家“宝藏公司”:就在投资者还在评判它的AKT赛道成果对公司估值的正向影响之时,它拿出了自主研发、有望用于增肌减脂的激活素受体II的抗体LAE102;当二级市场正在研究LAE102与GLP-1RA联用潜力时,这家公司又在NASH和抗肝纤维化领域展示出“独门秘籍”。
这家公司就是来凯医药(02105)。上周在美国举行的2024全球NASH-TAG大会上,它以壁报形式公布其自主研发的靶向激活的肝星状细胞的双功能NK-aHSC接合剂药物发现平台,以及基于该平台技术设计出来的LAE105抗体的抗肝纤维化临床前数据。
肿瘤、代谢、肝纤维化,这三个看似不相及的领域集成到一家biotech,却又如此顺理成章,这与公司创始人吕向阳博士及团队的科研背景、经历大有关联。
NASH治疗领域空白导致竞争异常激烈
据智通财经APP了解,在众多新药研发方向中,NASH相关靶向药物的研发一直以高门槛为全球业界所知。鉴于NASH领域巨大的临床需求和治疗空白,Evaluate Pharma曾预测2025年全球NASH药物的市场规模可达400亿美元。而纤维化程度的改善一直是衡量NASH药物有效性的关键指标之一。除了NASH适应症外,肝纤维化同样也是导致肝癌或肝功能衰竭的重要原因。
在此背景下,LAE105抗体作为一款改善肝纤维化,并可能应用于其它机理相似的纤维化疾病的一款潜在first-in-class新药,来凯医药有望凭借首次披露该药积极的临床前数据,进一步释放自身的内在价值。
值得一提的是,当前市场上的药物研发多集中在降低肝脂肪,或通过阻断肝星状细胞激活过程中的某个信号通路来缓解纤维化。
对比当前多技术路线的NASH在研药物疗效,目前市场大热的GLP-1类药物司美格鲁肽高剂量组效果不如Inventiva公司的泛PPAR激动剂;Akero公司FGF21类药物在公布的IIb期临床数据中显示肝脏纤维化改善同样不及预期。目前唯一可能率先“撞线”的是Madrigal公司的Resmetirom,这是一种口服小分子甲状腺激素受体-β(ΤRβ)激动剂,已获得了FDA加速批准和优先审批的认定。FDA能否在一季度批准Resmetirom作为第一个批准用于治疗NASH的药物上市,且拭目以待。
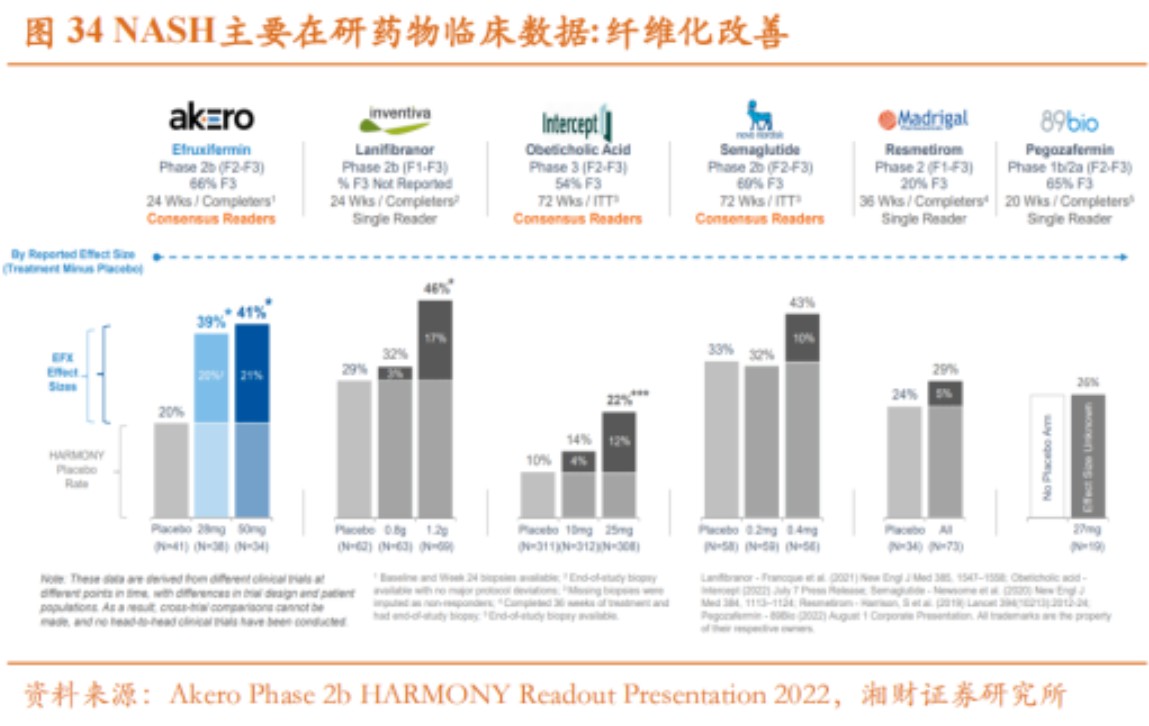
差异化创新让来凯有望实现纤维化治疗突破
相较之下,来凯医药另辟蹊径,期望通过利用自身免疫系统达成缓解纤维化的目的。
从作用机理来看,活化的肝星状细胞(aHSC)是肝肌成纤维细胞的主要来源,aHSC的积累也是肝纤维主要成因。此前,使用基因操作或药理学方法(如ADC,CAR-T)消耗aHSC已在各种动物模型中证明了抗纤维化作用。
为了将以上发现应用于临床,来凯医药可谓“六年磨一剑”,自主研发并建立起一个全球领先且独有的、利用人体自身免疫系统清除aHSC的药物发现平台。
在该技术平台支持下,来凯医药自主研发的LAE105在结合aHSC表面蛋白后可以招募和激活免疫细胞(如NK细胞),从而利用人体自身的免疫系统来清除aHSC,以此达到缓解肝纤维化的效果。除了改善肝纤维化,它还可能应用于其它机理相似的纤维化疾病,是一款潜在的first-in-class新药。而在未来,依托该平台,来凯也能够源源不断地持续开发未来更为优化的抗肝纤维化药物前体。
不仅在肝纤维化,活化的肌成纤维细胞在许多疾病(包括纤维化疾病、自身免疫性疾病和肿瘤)里都起着关键的致病作用。清除这类细胞在临床前动物模型里都展现出了药效。来凯的这一技术平台靶向性地清除肌成纤维细胞,其可应用前景广泛。
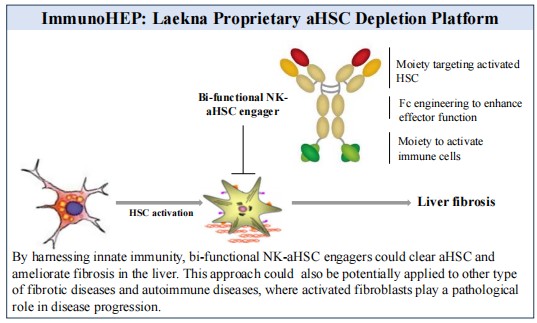
来凯独有的NASH科研优势
来凯在NASH和肝纤维化的科研积累并非一朝一夕。早在公司成立之初,创始人吕向阳博士就定下了这一战略方向,并为此建立起了大分子实验室和研发团队。
吕向阳博士曾是美国肝病研究学会的成员。他在诺华美国工作多年,于2007年回到上海参与建立诺华(中国)生物医学研究有限公司(CNIBR)。当时他力主诺华中国建立肝病新药研发平台,后出任项目研发负责人,从无到有组建起一支全球科研团队,进行了多项新药创新和转化医学研究。根据官方资料,他2012年还荣膺了诺华VIVA奖,获得“Novartis Leading Scientist”荣誉称号。
后来他离开诺华,创立了来凯医药,依然不忘初心。在他看来,肝病是中国人特有的高发疾病,全球NASH领域一直没有突破性药物。所以,他希望凭借来凯科研团队扎实的知识底蕴、全新的研发理念和独创的技术平台,加速肝纤维化新药的突破。
另一个关键人物,是来凯医药科学委员会顾问Scott L. Friedman 博士,现任美国纽约西奈山伊坎医学院治疗研发学院院长和肝病科主任。这位Friedman博士,正是全球最早分离和鉴定出肝星状细胞的学者之一。而此次本次壁报的作者之一、来凯早期研发团队生物高级总监张敏华博士也毕业于西奈山伊坎医学院。有Friedman博士这位大咖加持,来凯建立起清除aHSC的平台更加得心应手。
依托技术壁垒立足百亿蓝海,公司实现短中长期平衡
从市场角度来看,仅NASH治疗领域便有基数庞大的患者群体,大量的临床治疗需求未被满足。据弗若斯特沙利文预测,如果未来NASH药物新产品得以获批,那么2025年全球NASH药物市场将达到107亿美元,并于2030年达到322亿美元,期间复合年化增长率高达41.8%和24.6%。LAE105在减少肝纤维化的基础上,还可以和降肝脂的药物联用,从而实现对NASH更高效的疾病缓解。
纵观来凯医药近期的里程碑:
在临床进展方面,其核心产品afuresertib联合氟维司群的相关乳腺癌1b期临床试验数据已在圣安东尼奥乳腺癌大会发布,确认客观缓解率(ORR)达30%,中位无进展生存期 (PFS)达7.3个月,相比氟维司群单药治疗3-4个月的PFS接近翻倍,临床获益显著。目前公司已经开始启动III期关键试验。
在自主研发领域, LAE102是来凯自主研发的全球首创激活素受体II的抗体,2023年获得FDA的IND批准,中国CDE也受理了其新药临床试验申请,将初步评价LAE102的抗肿瘤活性和对于体重、肌肉量和脂肪量变化的影响。
而此次LAE105抗体连同NK-aHSC接合剂药物发现平台成功入选全球NASH-TAG大会,充分体现国际肝病研究学界对其研究成果的高度认可,也体现出LAE105抗体的创新含金量以及来凯硬核的研发实力。这无疑为来凯后续的顺利研发及最终的产品商业化进行了强有力背书。
用创始人吕向阳博士的话说,他希望来凯达到这样一个平衡——近期内企业有潜力上市的产品,在中远期有更具创新性的项目、突破性的创新药管线,形成一个健康的循环。



 扫码下载智通APP
扫码下载智通APP